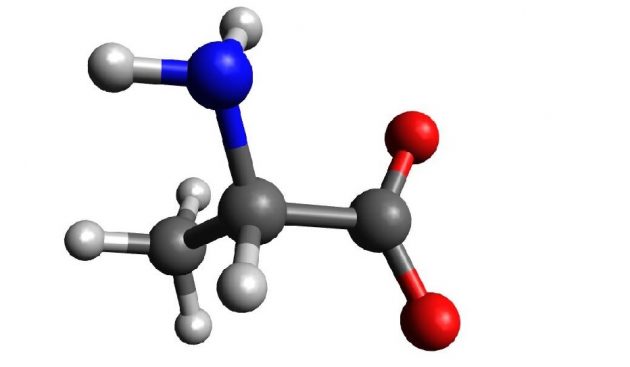
Os aminoácidos são substâncias orgânicas fundamentais para a formação das proteínas, usadas principalmente para fazer o processo de síntese. Depois da água, a proteína é o componente mais importante e de maior abundância nos seres vivos. Estima-se que o corpo humano tem da ordem 50.000 a 100.000 diferentes proteínas, cada uma com função específica e atuando de forma distinta. As proteínas são feitas a partir da junção de moléculas de aminoácidos. Para facilitar o entendimento dessa dinâmica, é possível pensar nos aminoácidos como a base de uma casa, como os tijolos; depois, a casa propriamente dita como as proteínas.
A partir de conhecimentos preliminares, um trabalho colaborativo buscou compreender a estrutura dos aminoácidos e propor modelos para a estrutura no ambiente natural e no ambiente biológico. O artigo publicado no Journal of Molecular Liquids foi produzido por dois pesquisadores do departamento de Física da Universidade Federal de Juiz de Fora (UFJF), em parceria com docentes da Universidade de São Paulo (USP) e da Universidade Federal de Goiás (UFG).
O estudo analisa a estabilidade e propriedades da molécula de L-alanina no estado neutro e quando carregado em água, a partir de um modelo de representação de fenômenos físicos. “A grande dificuldade é entender o ambiente natural, onde estas são normalmente encontradas. No ambiente biológico, a água, as outras moléculas e a temperatura induzem mudanças estruturais que não podem ser desprezadas. E mais do que isso, é graças a esse ambiente que ocorre a junção dos aminoácidos que por fim formarão a estrutura tridimensional das proteínas”, explica Valdemir Ludwig, primeiro autor do artigo, pesquisador e docente da UFJF.
Os modelos
Segundo Ludwig, os modelos procuram entender o efeito da água, as ligações de hidrogênio e a temperatura na estrutura da Alanina, um dos aminoácidos mais simples e abundantes na natureza. Anteriormente, outra pesquisa do grupo analisou os mesmos efeitos na molécula de Glicina. Além da investigação da parte estrutural, o trabalho também investiga as propriedades eletrônicas de cada unidade, fator que impacta significativamente no conhecimento sobre as proteínas.
“No nosso caso, estamos essencialmente preocupados em descrever as interações entre os átomos e moléculas num ambiente biofísico descritas por leis e princípios da física (lei de Coulomb, princípios da Mecânica Quântica, etc.). Usamos como ferramentas métodos numéricos, portanto os modelos são traduzidos em algoritmos que são executados em um ou vários computadores. Os resultados provém da análise das cargas eletrostáticas, da energia de equilíbrio, das estruturas das moléculas, das propriedades vibracionais”, descreve o pesquisador.
Aplicabilidade
O grande diferencial do modelo proposto consiste no fato de considerar, de maneira explícita, as moléculas do solvente, neste caso a água – o que permite a investigação das estruturas e das ligações de hidrogênio.
Dessa forma, em um ambiente neutro (que não é nem ácido, nem básico pela avaliação do pH), é observada a formação de ligações de hidrogênio da água com a alanina em uma dada energia média. Em ambientes mais ácidos, o número médio de ligações cai para menos da metade, em relação ao ambiente neutro. As análise demonstram, ainda, que em ambientes com pH maiores, considerados básicos, o número médio de ligações de hidrogênio não se modificou muito, mas a energia destas ligações reduziu, ou seja, apareceram como ligações mais fracas.
“O ambiente é composto por vários fatores como a temperatura, as moléculas de água, pH, concentração dos solventes. Em especial as moléculas de água podem favorecer a formação das proteínas. Um exemplo prático é a proteína que envolve o material genético do coronavírus, na água ela se forma e o vírus se reproduz. Mas se mudarmos o solvente para álcool, esta proteína se rompe, o material genético se perde e portanto o vírus deixa de existir. Podemos ver assim como dois solventes, induzem efeitos completamente opostos em um proteína”, afirma.
Há, ainda, a influência das propriedades físicas e químicas desses solventes – polaridade, calor específico, tensão superficial -, que são fatores que impactam na estrutura das proteínas. Além disso, a água, em especial, possui quase uma centena de propriedades, muitas delas ainda não compreendidas pela ciência moderna o que torna um grande desafio entender os efeitos da água em aminoácidos e por isso tem sido um campo com intensas pesquisas, diz o pesquisador. “A pesquisa básica tem essa característica, o produto principal é o conhecimento, e esse conhecimento servirá como base para a pesquisa aplicada poder desenvolver produtos que beneficiarão a sociedade”, complementa.